
L'ACTUALITÉ EN CANCÉROLOGIE VUE PAR GUSTAVE ROUSSY
Newsletter #10 - Juillet 2021
Essais précoces
Le digital drug-assignment priorise les cibles thérapeutiques

Stéphane Champiat, Daphné Morel, Loïc Verlingue
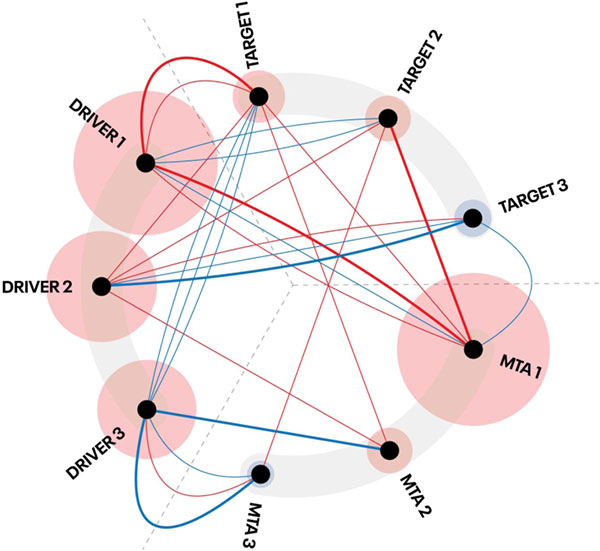
Le digital drug assignment (DDA, traduire par attribution numérique d’un traitement) fait partie de cette nouvelle tendance d’outils numériques d’aide à la décision thérapeutique personnalisée à partir de données moléculaires de tumeurs. Testé sur les données moléculaires issues de l’essai précoce SHIVA01, le DDA a pu identifier les patients pour lesquels une thérapie ciblée avait un impact positif (ou négatif) sur la survie sans progression.
La majorité des outils d’intelligence artificielle sont qualifiés de « boite noire » c’est-à-dire qu’il est difficile (voire impossible) de précisément cartographier le chemin de « réflexion » que va avoir la machine par rapport à une question donnée pour mener au résultat (prédiction). En d’autres termes, la machine est entrainée sur de nombreuses données pour arriver à prédire la réponse à une question précise – mais il est possible dans certains cas que sa décision soit essentiellement basée sur des détails qui paraitraient futiles à l’homme. C’est la raison pour laquelle les autorités restent actuellement très prudentes quant à l’utilisation d’outils d’intelligence artificielle dans le cadre d’essais cliniques interventionnels.
Dans cette étude, il n’en est rien. Les auteurs qualifient leur outil de « boite ouverte et transparente », puisque le modèle a été entrainé de telle sorte que ses choix doivent suivre les connaissances actuellement disponibles, obtenues via des sets de données expérimentales publiées et validées. Ainsi, le modèle ne devrait pas pouvoir prédire une issue qui irait à l’encontre de ce que sait « l’homme qui sait tout ».
Après avoir entrainé leur modèle sur ces databases publiques, les auteurs ont souhaité le valider en utilisant les données moléculaires des patients ayant été traités dans SHIVA. Ils ont montré que leur outil – qui fournit un score par patient par thérapie ciblée – était capable de différencier les patients présentant une maladie contrôlée sous traitement des patients présentant une progression sous traitement (p=0,037). Sur cette même cohorte, ils ont également observé que la survie sans progression médiane était plus élevée chez les patients présentant un score élevé, par rapport aux patients présentant un score bas (p=0,044).
C’est un petit pas de plus vers le modèle « parfait » qui pourrait réellement aider les cliniciens à faire des choix lorsque plusieurs options thérapeutiques existent pour un patient et qu’il faut prioriser les lignes de traitement. Si le cas demeure encore rare, l’explosion du nombre de médicaments ciblés disponibles (et autorisés) mènera nécessairement à ces situations d’ici quelques années.
Référence :
Petak I, et al. A computational method for prioritizing targeted therapies in precision oncology: performance analysis in the SHIVA01 trial. NPJ Precis Oncol. 2021 Jun 23;5(1):59.
Sénologie
La qualité de vie après un cancer du sein : on en parle !
Effets du traitement local du laser vaginal sur l'atrophie vulvo-vaginale chez les femmes atteintes d'un cancer du sein.
Anna Ilenko, Benjamin Verret
Les femmes atteintes d'un cancer du sein souffrent souvent d'une atrophie vulvo-vaginale (AVV) sévère qui entraîne à terme une mauvaise qualité de vie sexuelle et des troubles urinaires, majorés par les traitements oncologiques tels que la chimiothérapie ou l’hormonothérapie. L'une des études les plus importantes sur ce sujet, menée par une équipe de Gustave Roussy, a montré que la thérapie au laser sur l’atrophie vulvo-vaginale a augmenté la fonction sexuelle et la fonction urinaire avec des effets à long terme jusqu'à 18 mois après le traitement. Gustave Roussy se place comme un acteur majeur dans l’amélioration de la qualité de vie après-cancer, avec notamment le programme Interval.
Avec l’avancée des connaissances, la détection précoce du cancer du sein (CS), l’avènement de la médecine personnalisée et la progression des traitements, la survie après CS s’est nettement améliorée ces dernières années. La considération de la qualité de vie après cancer devient donc un élément majeur de prise en charge.
Dans cette étude prospective, il a été proposé aux femmes atteintes de CS et d’AVV de recevoir un traitement fractionné microablatif au laser CO2 intra vaginal une fois par mois pendant 3 mois. L'efficacité de la thérapie laser a été évaluée au départ, 6 mois et 18 mois après le traitement, en utilisant le score FSFI (Female Sexual Function Index), le score Ditrovie et le pH vaginal. 46 femmes atteintes de CS (âge médian 56,5 ans) ont été incluses entre mai et octobre 2018. Le niveau du pH a diminué au fil du temps (0,3 en moyenne à 18 mois, p = 0,02). La qualité de vie sexuelle a été significativement améliorée à 6 et à 18 mois (p < 0,0001). Le score total de Ditrovie s'est également amélioré à 6 mois (p = 0,01). Cette étude montre donc une amélioration de la qualité de vie significative après traitement par laser. D’autres études sont nécessaires pour déterminer le rythme de traitement par laser et la place des traitements topique dans l’AVV chez ces patientes atteintes de CS.
Les effets secondaires des traitements à long terme sont de plus en plus pris en compte comme le démontre le développement de cette technologie novatrice. En ce sens, le récent programme Interval (INTERaction soignants-patients, évaluation et VALidation des approches de soutien personnalisé dans l’amélioration de la qualité de vie des patients après un cancer), est menée par le Dr Ines Vaz Luis de Gustave Roussy. L’objectif est d’identifier les signatures prédictives de toxicités à long terme liées au traitement du cancer à long terme, de l’altération de la qualité de vie, dans le but de personnaliser les soins après un cancer.
Référence :
Veron, L., Wehrer, D., Annerose-Zéphir, G. et al. Effects of local laser treatment on vulvovaginal atrophy among women with breast cancer: a prospective study with long-term follow-up. Breast Cancer Res Treat 188, 501–509 (2021).
Hématologie
Cibler les monocytes malins pour traiter la leucémie myélomonocytaire chronique
Lucie Laplane, Iléana Antony-Debre, Aline Renneville
Dans les hémopathies myéloïdes chroniques, les cellules matures du clone favorisent l’expansion des cellules souches leucémiques. Sevin, Debeurme et al. ont identifié une combinaison thérapeutique qui, en restaurant l’apoptose des cellules leucémiques matures, constitue une approche thérapeutique innovante de la leucémie myélomonocytaire chronique, validée dans un modèle de xénogreffe.
Traditionnellement, dans les hémopathies malignes myéloïdes, les cellules souches leucémiques (CSL) sont considérées comme la cible de tout traitement ayant pour ambition l’éradication du clone malin. Les hémopathies myéloïdes chroniques se distinguent des leucémies aiguës par le fait que la différenciation des cellules hématopoïétiques est préservée, même si elle est déséquilibrée. Ces cellules matures du clone leucémique participent au microenvironnement des cellules souches leucémiques, et favorisent leur expansion aux dépens des cellules souches saines en produisant des cytokines inflammatoires.
La leucémie myélomonocytaire chronique (LMMC) est une hémopathie myéloïde chronique modèle car elle associe prolifération et dysplasie cellulaire. Le caractère prolifératif de la maladie aboutit à la production excessive de monocytes. Il n’y a pas de traitement curatif à l’exception de l’allogreffe de cellules souches hématopoïétiques saines, rarement possible du fait de l’âge avancé des patients et de leurs comorbidités.
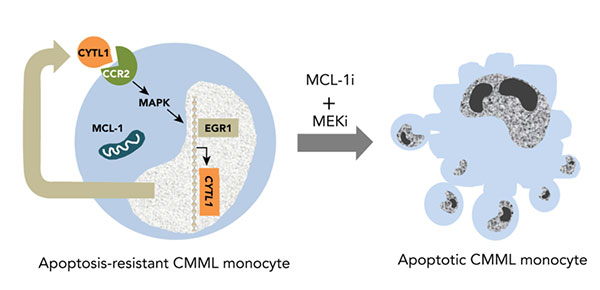
L’équipe du Pr Éric Solary s’est intéressée à ces monocytes présents en excès dans le sang des patients atteints de LMMC. Elle a identifié un défaut d’apoptose qui contribue à l’accumulation de ces monocytes. Ce défaut d’apoptose implique la protéine anti-apoptotique MCL-1. Les monocytes sécrètent en outre une cytokine appelée CYTL1, qui active la voie MAPK par un mécanisme autocrine ou paracrine. Dans un modèle murin de xénogreffe de cellules leucémiques issues de patients, l’association d’un inhibiteur de MCL1 à un inhibiteur de la voie MAPK restaure l’apoptose des monocytes et réduit l’infiltration leucémique.
Ces résultats suggèrent qu’une approche thérapeutique innovante ciblant non pas les cellules souches mais les cellules matures du clone leucémique devrait limiter l’expansion du clone malin.
Référence :
Sevin, Debeurme et al. Cytokine-like protein 1–induced survival of monocytes suggests a combined strategy targeting MCL1 and MAPK in CMML. Blood (2021) 137 (24): 3390–3402
Digestif
Le traitement des cancers du côlon avec mutation BRAF V600E reste un challenge
Michel Ducreux
L’étude MODUL est une étude de phase II testant différentes modalités de maintenance après induction de réponses par une chimiothérapie de type FOLFOX et bevacizumab pendant 8 cycles dans le traitement des cancers du côlon avec mutation BRAF V600E. La maintenance était ensuite définie en fonction des anomalies moléculaires mises en évidence pendant la phase d’induction.
Les résultats obtenus chez les 60 patients avec mutation BRAF V600E traités par 5FU bevacizumab ou Vemurafenib, 5FU et cetuximab ont été rapportés dans une présentation lors du dernier Esmo GI.
MODUL est une grande étude de phase II, dite adaptative, destinée à évaluer différentes maintenances après induction d’une réponse à 8 cycles de FOLFOX bevacizumab. Les résultats de la cohorte 2 des patients ne présentant pas de mutation BRAF avaient déjà été présentés : l’adjonction d’atezolizumab à la classique maintenance par 5FU + bevacizumab n’améliorait pas les résultats dans cette population.
A l’occasion de World Congress of GastroIntestinal Cancer, le Pr Michel Ducreux a présenté pour la première fois les résultats de la cohorte 1 qui a inclus 60 patients avec mutation BRAF V600E. Ces patients étaient randomisés entre traitement classique par 5FU bevacizumab ou triple association 5FU, vemurafenib, cetuximab. L’étude n’ayant inclus que 60 patients en randomisation, 2:1 n’a pas une puissance suffisante pour démontrer une supériorité du bras expérimental, qui semblait cependant donner des résultats peu différents du bras contrôle.
En revanche, l’intérêt majeur de cette étude, en dehors de la description d’un groupe de patients homogènes traités en première ligne pour une tumeur présentant cette mutation BRAF V600E observée dans 10 à 15% des cancers du côlon métastasés, est l’analyse translationnelle réalisée en parallèle et montrant que la pression exercée par l’anti-RAF et l’anti-EGFR induit des modifications de la tumeur avec activation de voies métaboliques à l’origine de résistance. Ces résultats sont très importants pour déterminer dans le futur des stratégies spécifiques à ces tumeurs agressives.
Référence :
M. Ducreux, J. Tabernero, A. Grothey, D. Arnold, P. O’Dwyer, M. Perdicchio, Z. Assaf, M. Das T. AQnn Oncol 2021hakur, N. Irahara, A. Tahiri, H. Schmoll, E. Van Cutsem, A. de Gramont. 5-FU/LV + cetuximab + vemurafenib as maintenance therapy for BRAF-mutant (BRAF mut) metastatic colorectal cancer: efficacy, safety, and exploratory biomarker findings from Cohort 1 of the MODUL trial O9 Ann Oncol 2021;32(S3):page S221.
Abonnez-vous à la newsletter Good to Know
Ne manquez pas les prochains numéros de la newsletter Good to Know : abonnez-vous !
Crédits photos : Adobe Stock, American Society of Hematology, Gustave Roussy.
