Les cellules CAR-T
Le traitement par cellules CAR-T (Chimeric Antigenic Receptor - T) ou CAR-T cells, est une stratégie d’immunothérapie cellulaire en plein développement, qui vise à combattre le cancer en s’appuyant sur le propre système immunitaire du patient.
Les cellules CAR-T sont des lymphocytes T modifiés génétiquement dans le but de reconnaître puis éliminer les cellules cancéreuses. Elles sont la base d’une toute nouvelle approche de traitement contre le cancer, consistant à prélever des cellules immunitaires d’un patient (ici, les lymphocytes T), pour les modifier génétiquement et les lui réinjecter.
Les lymphocytes T font partie d’une catégorie de globules blancs qui jouent un rôle très important pour les défenses de l’organisme. Ces cellules sont responsables de la réponse immunitaire cellulaire visant à détruire les agents pathogènes, aussi bien les bactéries que les cellules cancéreuses. Ils ont la capacité de reconnaître et détruire les cellules tumorales. Malheureusement, dans certains cas de cancer, ces dernières parviennent à les inactiver par différents mécanismes.
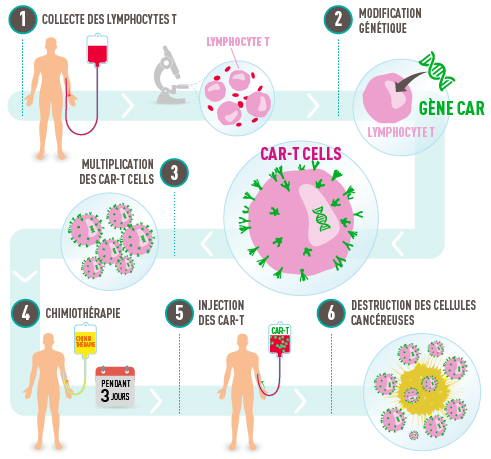
La production des cellules CAR-T commence par le prélèvement des lymphocytes T du propre patient que sont ensuite modifiés génétiquement afin qu’ils puissent reconnaître toute cellule cancéreuse. Pour cela, ils sont dans un premier temps collectés par leucaphérèse, un prélèvement sanguin ciblant les globules blancs. Après contrôle de leur qualité, ils subissent une modification génétique artificielle, on parle de modification ex vivo (en dehors de l’organisme). Le principe ? Produire, à l’aide d’un gène introduit dans leur noyau, des « récepteurs antigéniques chimériques » (CAR) à la surface des lymphocytes T. Grace à ce récepteur, les cellules CAR-T sont capables de reconnaître les cellules tumorales et de se fixer dessus. La modification génétique permet également d’introduire un élément de « costimulation » qui permet à la cellule CAR-T de s’activer et d’attaquer la cellule cancéreuse un fois fixée sur elle.
Une fois créées, les cellules CAR-T sont multipliées dans l’optique d’être administrées au patient. Avant l’injection, le patient reçoit durant trois jours une chimiothérapie dans le but d’affaiblir son système de défense immunitaire. Ainsi, en éliminant une partie des lymphocytes naturels, la multiplication des cellules CAR-T sera favorisée et le risque de rejet sera limité.
Une fois dans l’organisme, les cellules CAR-T vont donc reconnaître et cibler les cellules tumorales de manière spécifique grâce au récepteur CAR, puis s’activer contre elles et les éliminer.
Utilisation et axes de recherche
L’utilisation des cellules CAR-T représente un espoir thérapeutique pour les enfants et jeunes adultes atteints de leucémie aigüe lymphoblastique (LAL) mais également pour les adultes atteints de lymphomes diffus à grandes cellules B.
En effet, les études ont permis d’observer chez 40% de patients atteints d’un lymphome diffus à grandes cellules B, une réponse complète à la thérapie, sans progression de la maladie au bout de deux ans. Ces résultats sont prometteurs et très encourageants pour un traitement de 3è ligne. Le traitement par cellules CAR-T offre donc une alternative intéressante aux patients atteints de lymphomes en rechute ou réfractaires.
Gustave Roussy est autorisé depuis 2019 à traiter les patients par cellules CAR-T. Neuf patients y ont depuis été traités.
Des recherches sont en cours à l’Institut afin d’évaluer si les cellules CAR-T peuvent présenter un intérêt pour les lymphomes de hodgkin réfractaires et les myélomes multiples réfractaires. Enfin, des recherches sont menées sur des lymphocytes génétiquement modifiés (TCR) et les lymphocytes infiltrant la tumeur (TILS). Les TCR est les TILS sont en cours d’utilisation dans des essais cliniques pour le traitement de tumeurs solides et, ainsi, ouvrent une toute nouvelle voie de traitement pour des tumeurs réfractaires aux traitements classiques.
