
L'ACTUALITÉ EN CANCÉROLOGIE VUE PAR GUSTAVE ROUSSY
Newsletter #8 - Mai 2021
Focus ORL
Lambeau libre thoraco-dorsal avec nerf vascularisé : pas à pas d’une technique prometteuse
Nadia Benmoussa-Rebibo
Le lambeau libre perforant du pédicule thoraco-dorsal (TDAP) avec nerf vascularisé après parotidectomie élargie avec sacrifice du nerf facial est une technique inventée par le Dr Kolb à Gustave Roussy qui donne des résultats prometteurs sur la réinervation faciale. Le savoir-faire chirurgical de cette technique est explicité dans une vidéo pas à pas.
La chirurgie oncologique de la région parotidienne, en plus de la perte de substance qu’elle engendre, impose parfois le sacrifice du nerf facial qu’il faut idéalement reconstruire par une greffe nerveuse vascularisée. La reconstruction par un lambeau scapulo-dorsal comprenant le nerf moteur du latissimus dorsi vascularisé par le pédicule thoraco-dorsal apparait alors comme un choix idéal. L’objectif de cet article est d’expliquer, à l’aide d’une vidéo, la procédure chirurgicale utilisée à Gustave Roussy, afin de permettre aux chirurgiens reconstructeurs d’avoir tous les éléments techniques pour la reproduire.
Présentant le cas d’un malade de 16 ans, atteint d’un rabdomyosarcome de la région parotidienne, l’intervention a consisté en l’exérèse de la tumeur emportant la peau, la parotide et le nerf facial. La reconstruction a été effectuée par un lambeau perforant du pédicule thoraco-dorsal (TDAP), associé au prélèvement du nerf moteur vascularisé du latissimus dorsi, permettant d’anastomoser cinq branches principales du nerf facial.
La vidéo explicite les temps forts de cette chirurgie : installation du patient, prélèvement du lambeau, mise en place au niveau de la zone d’exérèse et anastomoses nerveuses. Les résultats fonctionnels seront illustrés à la fin de la vidéo par l’intermédiaire du cas clinique d’un malade de vingt-trois ans ayant bénéficié de cette technique après exérèse d’un carcinome adénoïde kystique parotidien.
Le lambeau chimérique scapulo-dorsal avec nerf vascularisé présente de nombreux avantages dans la réanimation faciale des patients atteints de cancers de la région parotidienne nécessitant le sacrifice du nerf facial. Il permet d’associer en un temps, la reconstruction des tissus mous et une greffe nerveuse vascularisée permettant ainsi de tenter de réhabiliter la motricité hémifaciale.
Référence :
Guyonvarch P, Benmoussa N, Moya-Plana A, Leymarie N, Mangialardi ML, Honart JF, Kolb F. Thoracodorsal artery perforator free flap with vascularized thoracodorsal nerve for head and neck reconstruction following radical parotidectomy with facial nerve sacrifice: a step-by-step surgical technique video. Head Neck. 2021 Apr 5. doi: 10.1002/hed.26701. Epub ahead of print. PMID: 33818833.
Ganglion sentinelle, nouveau standard thérapeutique pour les carcinomes débutants de la cavité orale
Antoine Moya-Plana
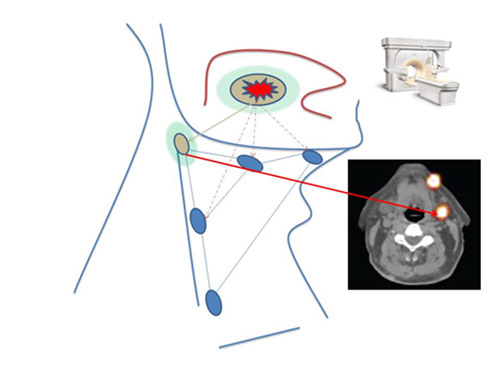
Une étude française multicentrique a permis de définir la technique du ganglion sentinelle comme le nouveau standard thérapeutique pour les carcinomes débutants de la cavité orale. Grâce à cette technique, permettant d’éviter un curage ganglionnaire à la plupart des patients, une diminution importante des effets secondaires du traitement chirurgical de ces cancers a été observée.
La technique du ganglion sentinelle (GS) permet de localiser et analyser avec précision le ou les ganglions lymphatiques reliés à une tumeur cancéreuse sans réaliser de manière systématique l’ablation de tous les ganglions de drainage. L’expertise de Gustave Roussy, dans ce domaine chirurgical, est reconnue sur le plan national et international. En chirurgie cervico-faciale, les résultats carcinologiques de cette procédure pour le traitement des carcinomes débutants (T1-T2N0) de la cavité orale et de l’oropharynx n’ont jamais été comparés à ceux d’un curage ganglionnaire systématique, qui constitue le traitement de référence.
Cette étude multicentrique, française, de phase III, a ainsi randomisé 307 patients en deux groupes : (1) curage systématique ou (2) ganglion sentinelle (éventuellement complété par un curage en cas de GS envahi).
Les résultats carcinologiques évalués par le taux de survie sans récidive à 2 ans et 5 ans étaient similaires dans les deux groupes. Le taux de récidive ganglionnaire cervicale à 2 ans était également comparable (89.6 % vs 90.7 %). En revanche, la durée moyenne d’hospitalisation était significativement plus courte dans le groupe GS (7 jours vs 8 jours) tandis que les patients du groupe « curage systématique » présentaient des résultats fonctionnels moins bons à 6 mois post-opératoires, notamment en termes de mobilité de l’épaule.
Cette étude démontre, dans la prise en charge des carcinomes débutants de la cavité orale, la sécurité carcinologique de la technique du ganglion sentinelle associée à une diminution des séquelles post-thérapeutiques. Elle établit ainsi un nouveau standard de traitement.
Les résultats de cette étude ont été détaillés, en présentation orale, à l’ASCO 2020 puis publiés dans le Journal of Clinical Oncology.
Références :
1. Garrel R, Poissonnet G, Moya-Plana A, et al. Fakhry N, Dolivet G, Lallemant B, et al. Equivalence Randomized Trial to Compare Treatment on the Basis of Sentinel Node Biopsy Versus Neck Node Dissection in Operable T1-T2N0 Oral and Oropharyngeal Cancer. J Clin Oncol. 2020 Dec 1;38(34):4010-4018. doi: 10.1200/JCO.20.01661.
2. Garrel R, Poissonnet G, Moya Plana A, et al. Sentinel node biopsy stands the test of time and the proof of time.Eur Ann Otorhinolaryngol Head Neck Dis. 2021 Jan;138(1):5-6. doi: 10.1016/j.anorl.2020.11.013. Epub 2020 Dec 10.
Hématologie
LAL Ph+ : vers un traitement sans chimiothérapie ?
Florence Pasquier
Le pronostic des leucémies aiguës lymphoblastiques à chromosome Philadelphie (LAL Ph+) a été transformé suite au développement d’inhibiteurs spécifiques. Leur association récente avec des anticorps monoclonaux bi-spécifiques permet de traiter les LAL Ph+ sans chimiothérapie, de manière efficace et peu toxique.
Les leucémies aiguës lymphoblastiques à chromosome Philadelphie (LAL Ph+) sont des cancers rares de la moelle osseuse. Leur pronostic, considéré comme défavorable en raison de résistance à la chimiothérapie conventionnelle, a été transformé suite au développement d'inhibiteurs spécifiques, les inhibiteurs de tyrosine kinase (ITK). Plus récemment, des anticorps monoclonaux dits bi-spécifiques (se fixant sur les lymphocytes T cytotoxique CD3+ et les lymphocytes B pathologiques CD19+) y ont été associés. Ces traitements permettent d’obtenir d’excellentes réponses, tout en diminuant la quantité de chimiothérapie administrée et donc les effets secondaires.
Dans cette étude de phase 2, menée par le groupe italien GIMEMA, 63 patients atteints de LAL Ph+ ont reçu des corticoïdes en association à un ITK, le dasatinib, administré par voie orale, et à un traitement d’immunothérapie, le blinatumomab, administré par voie intraveineuse. Après un cycle, 98 % des patients étaient en rémission complète. 21 patients ont pu bénéficier d’une greffe de cellules souches hématopoïétiques, qui permet de prévenir les rechutes. Après un an et demi, 95 % des patients étaient vivants et 88 % toujours en rémission. La tolérance était bonne, les effets secondaires de ces molécules étant connus, ils sont soit prévenus, soit gérés par un traitement symptomatique ou une modification de posologie. En conséquence, les durées d’hospitalisation sont réduites et la prise en charge est majoritairement ambulatoire. Cependant, des rechutes neurologiques ainsi que l'émergence de cellules résistantes au dasatinib ont été observées. Cela souligne l'importance du choix de l’ITK, tous ne présentant pas le même risque de sélection de clones résistants, et pose la question de savoir si l'on pourra se passer totalement de la chimiothérapie conventionnelle.
Cet article illustre donc le développement actuel de thérapeutiques anticancéreuses basées sur des traitements ciblés et sans chimiothérapie.
Référence :
Foà R, Bassan R, Vitale A, Elia L, Piciocchi A, Puzzolo MC, Canichella M, Viero P, Ferrara F, Lunghi M, Fabbiano F, Bonifacio M, Fracchiolla N, Di Bartolomeo P, Mancino A, De Propris MS, Vignetti M, Guarini A, Rambaldi A, Chiaretti S; GIMEMA Investigators. Dasatinib-Blinatumomab for Ph-Positive Acute Lymphoblastic Leukemia in Adults. N Engl J Med. 2020 Oct 22;383(17):1613-1623. doi: 10.1056/NEJMoa2016272.
Recherche
Le régime cétogène : nouvel allié face au cancer ?
Gladys Ferrere, Marion Picard
Une étude européenne publiée dans la revue Journal of Clinical Investigation INSIGHT par des chercheurs de Gustave Roussy, de différentes universités françaises (Paris-Saclay, Paris-Sorbonne, Aix-Marseille, Orléans), italiennes (Trieste et Trente) et anglaises (King’s College London) démontrent l’importance de l’alimentation dans le succès des immunothérapies.
Bien que des traitements innovants comme l’immunothérapie aient permis une amélioration dans la prise en charge de nombreux cancers agressifs (mélanome, cancer pulmonaire et rénale), la majorité des patients répondent peu ou pas à ces traitements. Un des enjeux prédominants en cancérologie est donc de contourner cette résistance aux immunothérapies.
Peu d’informations existent sur l’influence de facteurs environnementaux (tel que la nutrition) sur la balance délicate entre microbiote, système immunitaire, métabolisme et la réponse aux immunothérapies.
Récemment, une étude menée au sein de l’équipe de la Pr Zitvogel a montré que la mise en place d’un régime cétogène (caractérisé par une diminution de l’apport en sucres et favorisant l’utilisation par l’organisme de corps cétoniques comme source d’énergie) permettait de restaurer l’efficacité des immunothérapies chez des modèles animaux atteint de cancers agressifs. Ce contrôle de la croissance tumorale s’accompagne d’un remodelage du système immunitaire en faveur d’un environnement anti-tumorigène ainsi que de l’apparition de signatures microbiennes et métaboliques spécifiques.
De façon intéressante, l’équipe a mis en évidence que le simple ajout du corps cétonique 3-hydroxybutyrate (3-HB), dans l’alimentation classique des animaux amenait aux mêmes observations, et ce même lorsque l’apport en 3-HB est intermittent.
Ces résultats novateurs montrent pour la première fois un effet important de l’alimentation sur la surveillance antitumorale, notamment à travers des modifications du système immunitaire et du microbiote.
Le régime cétogène, bien que très prometteur, présente peu d'appétence pour les patients et peut-être potentiellement toxique pour le système cardiovasculaire. Ainsi, l’emploi d'un corps cétonique comme le 3-HB en complément d’une alimentation classique représente une option plus facile à mettre en place et à respecter pour les patients. Cela faciliterait alors l’intégration de ce support nutritionnel dans les thérapies anticancéreuses.
Référence :
Gladys Ferrere, Maryam Tidjani Alou, Peng Liu, Anne-Gaëlle Goubet, Marine Fidelle, Oliver Kepp, Sylvère Durand, Valerio Iebba, Aurélie Fluckiger, Romain Daillère, Cassandra Thelemaque, Claudia Grajeda-Iglesias, Carolina Alves Costa Silva, Fanny Aprahamian, Déborah Lefevre, Liwei Zhao, Bernhard Ryffel, Emeline Colomba, Monica Arnedos, Damien Drubay, Conrad Rauber, Didier Raoult, Francesco Asnicar, Tim Spector, Nicola Segata, Lisa Derosa, Guido Kroemer and Laurence Zitvogel. Ketogenic diet and ketone bodies enhance the anticancer effects of PD-1 blockade. JCI Insight. 2021 Jan 25; 6(2): e145207. doi: 10.1172/jci.insight.145207
Digestif
La dosimétrie personnalisée optimise la radiothérapie interne sélective dans le carcinome hépatocellulaire non résécable
Léonor Benhaim
L’étude Dosisphere-01 (phase II) a montré que la dosimétrie personnalisée permettait d’adapter efficacement la dose administrée comparativement à une dosimétrie standardisée. Cette étude est positive sur son critère de jugement principal puisque le taux de réponse objective était de 71 % à 3 mois en cas de dosimétrie personnalisée contre 36 % pour une dosimétrie standard (p=0,0074).
La radiothérapie interne sélective (SIRT) est utilisée pour le traitement du carcinome hépatocellulaire (CHC) non résécable. Elle consiste en l’administration intra-artérielle hépatique de microsphères de verre chargées à l’yttrium-90.
Les études de phase III n’ont pas montré de supériorité en termes de survie globale de ce traitement comparé au traitement systémique par Sorafénib (SARAH, Sirvenib). La SIRT reste cependant une bonne alternative thérapeutique en raison de sa bonne tolérance.
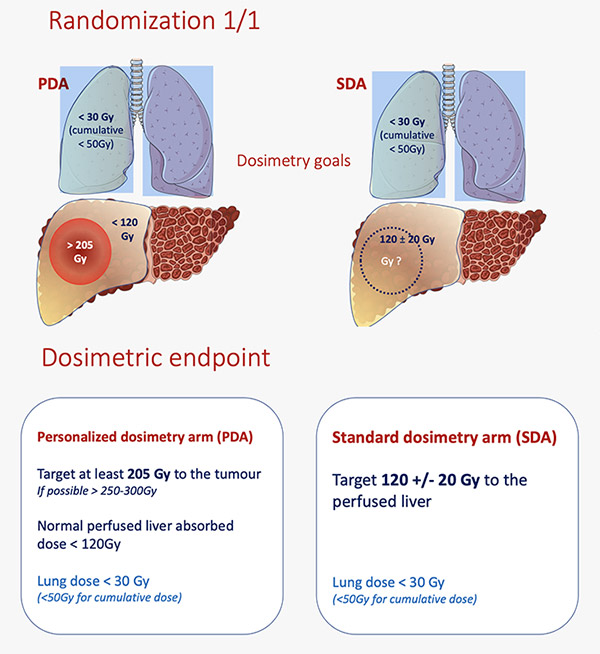
Le traitement par SIRT est toujours composé d’une phase de planification de traitement par dosimétrie pour caractériser les fixations des lésions et éliminer des contre-indications. La dosimétrie personnalisée permet d’assurer qu’une dose minimale de 205 Gy soit administrée sur la cible tumorale tout en respectant les critères de sécurité. La dose reçue par la tumeur en dosimétrie standard étant située autour de 120 Gy.
Dosisphere-01 est une étude de phase de II menée dans quatre centres français dont Gustave Roussy, auprès de l’équipe de radiologie interventionnelle. Le Pr Thierry de Baere et le Dr Lambros Tselikas ont ainsi largement participés aux inclusions dans cette étude qui est la première étude randomisée dédiée au sujet de la dosimétrie. Les patients étaient randomisés entre une dosimétrie standard ou personnalisée.
Cette étude a montré la supériorité de la personnalisation avec une augmentation significative des taux de réponse objective : 71 % à 3 mois contre 36 % pour une dosimétrie standard (p=0,0074). La tolérance au traitement était meilleure dans le groupe dosimétrie personnalisée. Les effets secondaires sévères étaient de 20 % dans le groupe dosimétrie personnalisée contre 33 % dans le groupe dosimétrie standard.
Cette étude impose donc un changement de pratique clinique avec dosimétrie personnalisée systématique pour offrir au patient le traitement avec le meilleur rapport bénéfice-risque dans le traitement du CHC non opérable.
Les futures études sur la SIRT devraient proposer une dosimétrie personnalisée systématique pour assurer la validité de leurs résultats.
1. Vilgrain V, Pereira H, Assenat E, Guiu B, Ilonca AD, Pageaux GP, Sibert A, Bouattour M, Lebtahi R, Allaham W, Barraud H, Laurent V, Mathias E, Bronowicki JP, Tasu JP, Perdrisot R, Silvain C, Gerolami R, Mundler O, Seitz JF, Vidal V, Aubé C, Oberti F, Couturier O, Brenot-Rossi I, Raoul JL, Sarran A, Costentin C, Itti E, Luciani A, Adam R, Lewin M, Samuel D, Ronot M, Dinut A, Castera L, Chatellier G; SARAH Trial Group. Efficacy and safety of selective internal radiotherapy with yttrium-90 resin microspheres compared with sorafenib in locally advanced and inoperable hepatocellular carcinoma (SARAH): an open-label randomised controlled phase 3 trial. Lancet Oncol. 2017 Dec;18(12):1624-1636. doi: 10.1016/S1470-2045(17)30683-6.
2. Garin E, Tselikas L, Guiu B, Chalaye J, Edeline J, de Baere T, Assenat E, Tacher V, Robert C, Terroir-Cassou-Mounat M, Mariano-Goulart D, Amaddeo G, Palard X, Hollebecque A, Kafrouni M, Regnault H, Boudjema K, Grimaldi S, Fourcade M, Kobeiter H, Vibert E, Le Sourd S, Piron L, Sommacale D, Laffont S, Campillo-Gimenez B, Rolland Y; DOSISPHERE-01 Study Group. Personalised versus standard dosimetry approach of selective internal radiation therapy in patients with locally advanced hepatocellular carcinoma (DOSISPHERE-01): a randomised, multicentre, open-label phase 2 trial. Lancet Gastroenterol Hepatol. 2021 Jan;6(1):17-29. doi: 10.1016/S2468-1253(20)30290-9.
Gynécologie & génito-urinaire
La nouvelle association lenvatinib pembrolizumab : l’association VEGFR TKI-ICI pour toutes les tumeurs ?
Emeline Colomba, Laurence Albiges
Le lenvatinib est un antiangiogénique, inhibiteur de tyrosines kinases multicible. Il inhibe les trois principaux récepteurs du facteur de croissance endothélial vasculaire VEGFR1, 2 et 3, ainsi que les récepteurs du facteur de croissance des fibroblastes (FGFR) 1, 2, 3 et 4, et le récepteur du facteur de croissance dérivé des plaquettes (PDGFR)α, c-Kit et le proto-oncogène RET. Le pembrolizumab est un anticorps monoclonal humanisé qui se lie au récepteur PD-1 (programmed cell death-1).
L’association lenvatinib et pembrolizumab s’est imposée récemment comme un nouveau standard dans le cancer du rein métastatique en première ligne et dans le cancer de l’endomètre métastatique en 2e ligne post chimiothérapie à base de sels de platine.
En février 2021, les résultats de l’étude de phase 3 CLEAR ont ajouté un nouveau standard en première ligne dans le cancer du rein métastatique en démontrant l’efficacité de l’association lenvatinib pembrolizumab. Dans cet essai de phase 3, les patients étaient randomisés entre l’association lenvatinib (20 mg par voie orale une fois par jour) plus pembrolizumab (200 mg par voie intraveineuse une fois toutes les 3 semaines) versus l’association lenvatinib (18 mg par voie orale une fois par jour) plus évérolimus (5 mg par voie orale une fois par jour) versus (vs) le standard historique, le sunitinib (50 mg en alternant 4 et 2 semaines sans traitement).
L’association lenvatinib plus pembrolizumab était associée significativement à un bénéfice en survie globale (SG), en survie sans progression (SSP) et en taux de réponse objectif (TRO) en comparaison au sunitinib. La SSP médiane était remarquablement longue avec 24 mois versus 9 mois sous sunitinib (HR : 0,39; 95 % [CI], 0,32 to 0,49; P<0,001. La SG était significativement plus longue versus sunitinib (HR : 0,66; 95 % CI, 0,49 to 0,88; P=0,005). Le taux de réponse objective de 71 %, comprenant 16 % de réponses complètes, vs un taux de réponse de 36 % sous sunitinib. On notait 82 % d’effets secondaires de grade 3-4 (diarrhées et HTA essentiellement) vs 72 % sous sunitinib.
L’essai CLEAR est la 4e étude de phase 3 rapportant un bénéfice en survie globale en première ligne dans le cancer du rein métastatique avec une combinaison après les associations Nivolumab-Ipilimumab, axitinib pembrolizumab, toutes deux disponibles en France et l’association cabozantinib nivolumab plus récemment rapportée.
La combinaison lenvatinib et pembrolizumab apparait comme un nouveau standard de soin particulièrement efficace avec pour la première fois dans le cancer du rein métastatique une SSP de près de 2 ans en première ligne. L’association lenvatinib - pembrolizumab est en cours d’évaluation dans les carcinomes rénaux non à cellules claires (étude MK-3475-B61) et représente le nouveau bras standard d’études de triplets en 1re ligne (étude MK-6482-012), ces études sont en cours d’activation en France.
En mars 2021, l'étude de phase 3 309/ KEYNOTE 75-775 a démontré avec la même association pour la première fois un bénéfice en survie globale en 2e ligne dans le cancer de l’endomètre métastatique en progression après chimiothérapie à base de sel de platine. Les patientes étaient randomisées entre lenvatinib (20 mg par voie orale une fois par jour) plus pembrolizumab (200 mg par voie intraveineuse une fois toutes les 3 semaines) vs une monochimiothérapie aux choix de l’investigateur par doxorubicine 60 mg/m2 J1=J21 ou du taxol hebdomadaire 80 mg/m2, le standard de soin de l’époque. Les patientes étaient stratifiées sur le statut microsatellite de leur tumeur réalisé en centralisé : tumeur stable (MSS) ou instable (MSI). L’étude était positive en termes de SG, SSP et TRO en comparaison à la monochimiothérapie.
Chez toutes les patientes (MSS et MSI) après un suivi de 11 mois, la SG était augmentée sous lenvatinib pembrolizumab : 18,3 vs 11,4 mois sous chimiothérapie ; HR 0,62; 95 % CI 0,51-0.75; P<0,001). La SSP médiane et le TRO était doublés : 7,2 vs 3,8 mois; HR 0,56; 95 % CI 0,47-0,66; P<0,001 et un TRO de 32 % vs 14,7 % sous monochimitohérapie; P<0,001).
Chez les patientes MSS, le bénéfice était conservé, la SSP médiane sous lenvatinib plus pembrolizumab était de 6,6 vs 3,8 mois sous monochimiothérapie; HR à 0,60; 95 % [CI] 0,50-0,72; P<0,001; La SG était également plus longue: 17,4 vs 12,0 mois ; HR 0,68; 95 % CI 0,56-0,84; P<0,001. On notait 88,9 % d’effets secondaires de grade 3-4 sous lenvatinib plus pembrolizumab versus 72,7 % sous monochimiothérapie.
Cette combinaison très prometteuse en termes d’efficacité est en cours d’exploration dans de nombreuses études de phase 3 notamment dans le cancer de vessie, du poumon et dans le carcinome hépatocellulaire. Elle remplacera peut-être un jour la chimiothérapie dans certaines tumeurs offrant un contrôle de la maladie optimale et prolongée. Elle représentera en revanche un challenge pour les oncologues en termes de gestion des effets secondaires et d’optimisation des soins de support.
Références :
1. Robert J. Motzer, Camillo Porta, Masatoshi Eto, Thomas Powles, Viktor Grünwald, Thomas E. Hutson, Boris Alekseev, Sun Young Rha, Evgeny Kopyltsov, María José Méndez Vidal, Sung-Hoo Hong, Anil Kapoor, Teresa Alonso Gordoa, Jeffrey C. Goh, Jaime R. Merchan, Alan D. Smith, Kalgi Mody, Rodolfo F. Perini, Dongyuan Xing, and Toni K. Choueiri. Phase 3 trial of lenvatinib (LEN) plus pembrolizumab (PEMBRO) or everolimus (EVE) versus sunitinib (SUN) monotherapy as a first-line treatment for patients (pts) with advanced renal cell carcinoma (RCC) (CLEAR study). Journal of Clinical Oncology 2021 doi: 10.1200/JCO.2021.39.6_suppl.269
2. Makker V, Colombo N, Casado Herráez A, et al: A multicenter, open-label, randomized phase 3 study to compare the efficacy and safety of lenvatinib in combination with pembrolizumab vs treatment of physician’s choice in patients with advanced endometrial cancer: Study 309/KEYNOTE-775. Society of Gynecologic Oncology 2021 Virtual Annual Meeting on Women’s Cancer. Abstract 37/ID 11512. Presented March 19, 2021.
Abonnez-vous à la newsletter Good to Know
Ne manquez pas les prochains numéros de la newsletter Good to Know : abonnez-vous !
Crédits photos : Adobe Stock, Gustave Roussy.
