Groupe Espèces Réactives de l’Oxygène et Radiocarcinogenèse
Ce groupe est rattaché à l'équipe Recombinaison Réparation de l'ADN, ROS et Cancer
Les NADPH oxydases ( 5 NOXs et 2 DUOXs), découvertes au début des années 2000, sont des protéines membranaires avec une production de ROS très contrôlée. La thyroïde exprime trois de ces NADPH oxydases (cf Figure) :
- DUOX1 dont le rôle est inconnu,
- DUOX2 clonée par notre équipe qui fournit l’H2O2 nécessaire à la TPO pour la biosynthèse des hormones thyroïdiennes
- NADPH oxydase NOX4
En produisant de l’H2O2, les NADPH oxydases DUOX1 et DUOX2, actives sur la membrane plasmique apicale du thyrocyte, et NOX4, exprimée sur la membrane de différents compartiments cellulaires (réticulum endoplasmique, noyau, mitochondrie ..), sont suspectées d’être impliquées dans la radiocarcinogenèse et tumorigenèse thyroïdienne.
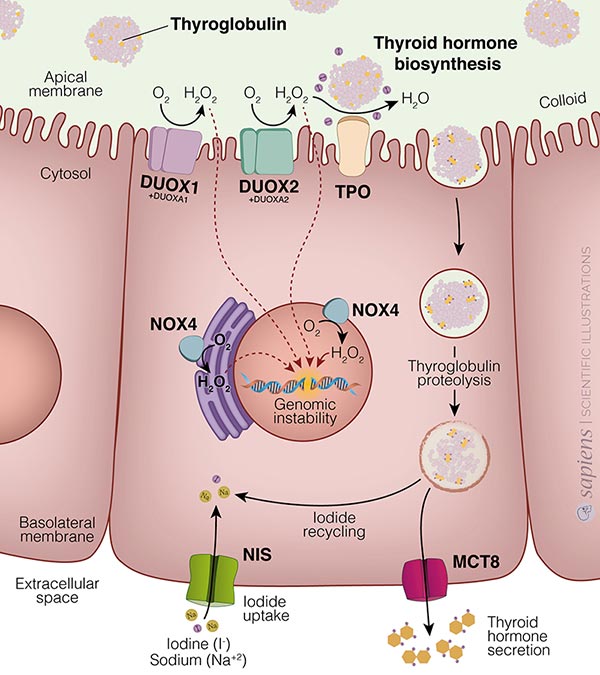
Fig : Rôle des NADPH oxydases dans la radiocarcinogenèse
- Rôle des ROS et des NADPH oxydases dans la radiocarcinogenèse
Une des origines connues du cancer thyroïdien est l'exposition durant l’enfance aux rayonnements ionisants. Plus de 90% de ces cancers sont de type papillaires présentant dans 70% des cas le réarrangement RET/PTC1. Ce réarrangement peut être induit par les ROS. Nos données récentes montrent que la NADPH oxydase DUOX1, induite à post-irradiation (post-IR), provoque un stress oxydatif chronique à l'origine de dommages persistants à l'ADN. Les deux gènes impliqués dans le réarrangement RET/PTC1 sont tous deux situés dans des sites fragiles chromosomiques, lesquels peuvent casser lors d’un stress réplicatif. Il y a maintenant des évidences que le stress réplicatif et le stress oxydatif sont liés et se renforcent mutuellement.
Avec des modèles cellulaires et animaux et une technologie « Etat de l’Art », nous avons entrepris de disséquer les événements moléculaires et mécanistiques induits par les ROS qui contribuent à l'instabilité génomique et à la radiocarcinogenèse.
- Rôle des NADPH oxydases dans la régulation de l’expression du transporteur de l’iode (NIS
La perte d’expression du transporteur de l’iode (NIS) est un événement précoce de l’oncogenèse thyroïdienne. Les mécanismes moléculaires assurant le contrôle de son expression sont encore mal connus. Sur un plan clinique, certains cancers de la thyroïde porteurs de la mutation BRAF concentrent l’iode 131 de manière insuffisante pour pouvoir bénéficier de la radiothérapie métabolique. Des résultats récents montrent que NOX4, induite par l’oncogène BRAFV600E, contrôle l’expression du gène codant NIS (manuscrit soumis). Notre objectif est de définir le rôle de NOX4 en tant que système générateur de ROS dans les mécanismes redox qui conduisent à l’altération de l’expression du transporteur de l’iode (NIS) dans les cellules tumorales.
Nos travaux se font en étroite collaboration avec la recherche clinique dirigée par Martin Schlumberger (PU-PH).
